Уравнение Аррениуса
Уравнение Аррениуса рассчитывает константу скорости реакции (k). В условиях фиксированной температуры химическая реакция возможна, если молекулы обладают энергией активации. Активированные молекулы взаимодействуют посредством столкновений.
Частота столкновений (A) зависит от температуры. Следовательно, скорость химической реакции зависит от Ea. Где Ea – энергия активации. Чем больше данный показатель, тем меньше скорость реакции, так как количество активных взаимодействующих молекул меньше.
Соответственно, чем меньше Ea, тем быстрее скорость химической реакции. Из этого вытекает, что если Ea = 0, то химическая реакция протекает практически мгновенно.
Для чего необходим расчет уравнения Аррениуса? Константа (k) взаимосвязана с Ea. Если Ea в пределах от 50 до 100 кДж∙моль-1, то при изменении температуры на 10⁰, скорость реакции изменяется в пределах 2-4 раз.
Рассчитать константу (k) скорости реакции по уравнению Аррениуса можно с помощью онлайн калькулятора. Зная данные:
• температура;
• частоту столкновений взаимодействующих молекул (k);
• энергию Ea,
можно вывести константу скорости химической реакции. Исходя из анализа данных, можно определить, что ускорение химической реакции возможно двумя способами: увеличить температуру, снизить Ea.
Пожалуйста напишите с чем связна такая низкая оценка:
«На главный экран»
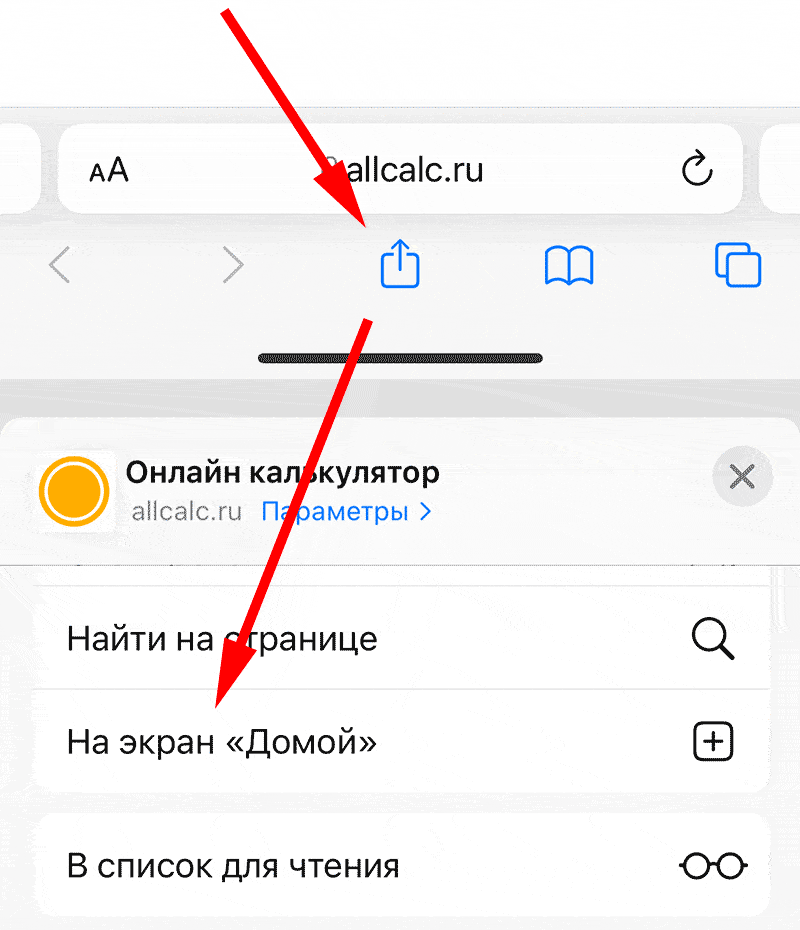
«На главный экран»